In der vorliegenden Arbeit wurde Datenmaterial analysiert, das eine mögliche Wirkung von Melatonin auf den Knochenstoffwechsel und die entsprechenden Auswirkungen auf die Ätiologie und Behandlung von Knochenerkrankungen wie Osteoporose und adoleszente idiopathische Skoliose (AIS) untermauert. Melatonin kann über Mechanismen, an denen sowohl von Melaninrezeptoren vermittelte als auch rezeptorunabhängige Abläufe beteiligt sind, den Knochenabbau verhindern und die Knochenneubildung fördern.
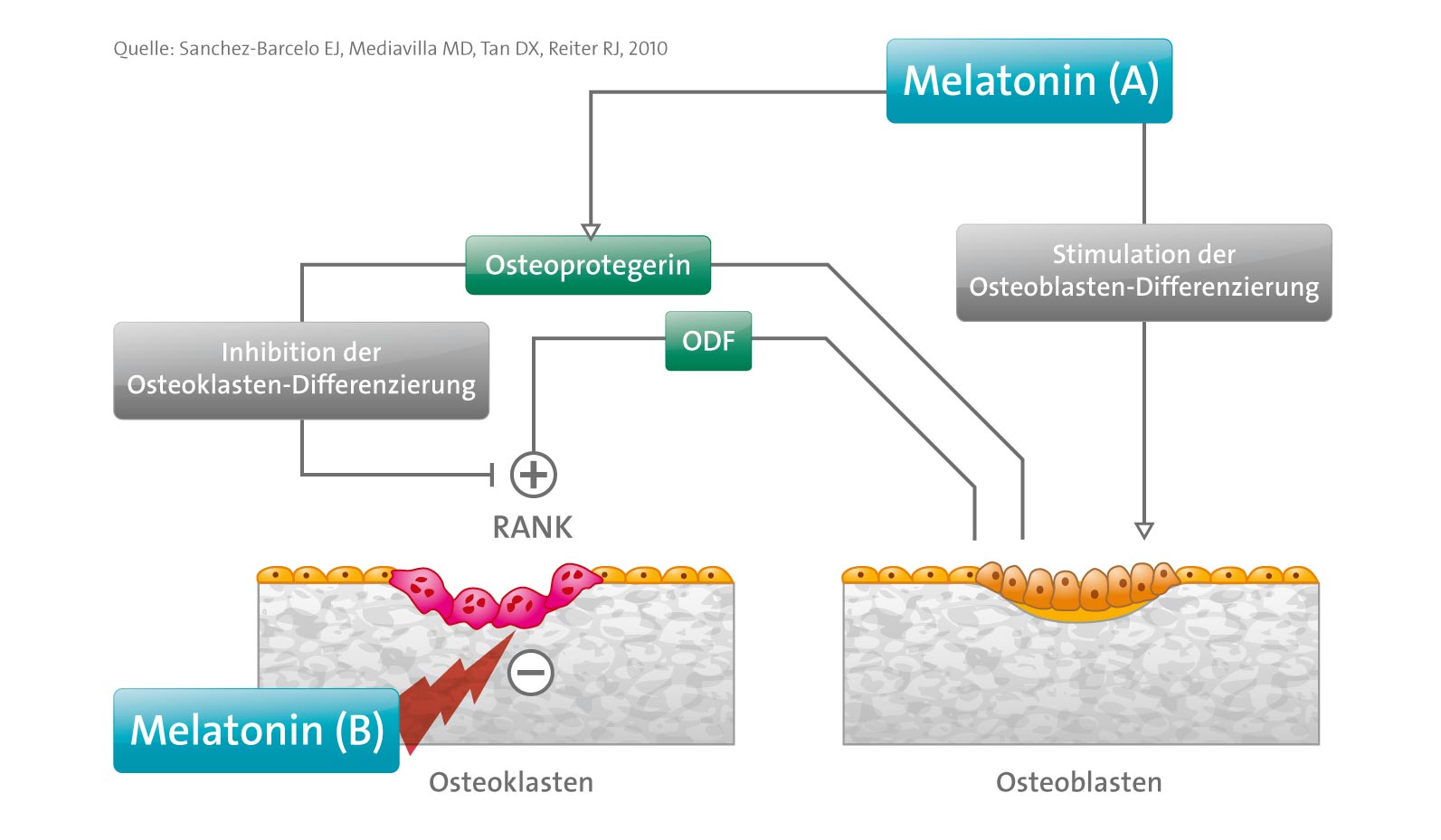
Die drei wichtigsten Wirkmechanismen von Melatonin auf die Knochenfunktion könnten sein:
- Förderung der Differenzierung und Aktivität der Osteoblasten;
- gesteigerte Expression von Osteoprotegerin in den Osteoblasten, wodurch die Differenzierung der Osteoklasten verhindert wird;
- Neutralisierung der freien Radikale, die durch die Osteoklastenaktivität generiert werden und für die Knochenresorption verantwortlich sind.
Verschiedene In-vitro- und In-vivo-Experimentalstudien (mit teils widersprüchlichen Ergebnissen) weisen auf eine mögliche Rolle von Melatonindefiziten in der Ätiologie von Osteoporose und AIS hin und eröffnen einen neuen Einsatzbereich von Melatonin als potenzielles Therapeutikum in der Behandlung dieser Knochenerkrankungen.